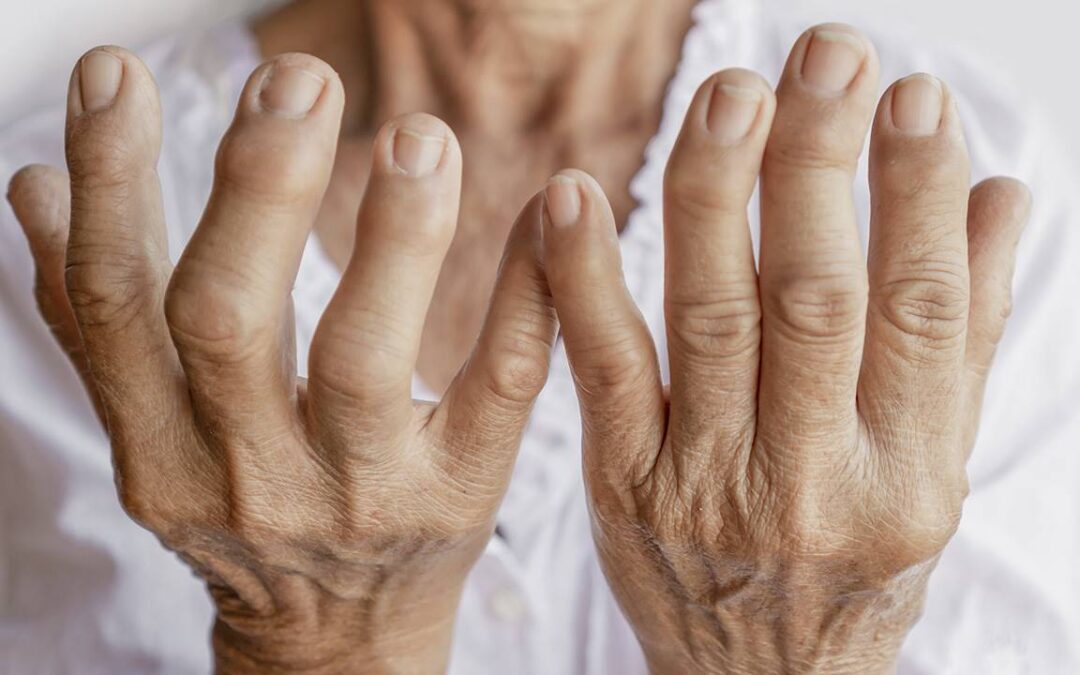
Reumatoïde artritis
Reumatoïde artritis is een chronische systemische auto-immuunziekte die voornamelijk de gewrichten aantast. Reumatoïde artritis produceert laesies die worden gemedieerd door cytokines, chemokines en metalloproteasen. Perifere gewrichten (bijv. polsen, metacarpofalangeale gewrichten) zijn symmetrisch ontstoken, bijna altijd resulterend in progressieve vernietiging van gewrichtsstructuren, meestal vergezeld van systemische symptomen. De diagnose vereist specifieke klinische, laboratorium- en radiologische criteria. De behandeling omvat medicijnen, fysiotherapeutische maatregelen en soms een operatie. Ziektemodificerende antireumatische geneesmiddelen helpen de symptomen onder controle te houden en de progressie van de ziekte te vertragen.
Reumatoïde artritis treft ongeveer 1% van de bevolking. Vrouwen worden 2 tot 3 keer vaker getroffen dan mannen. De ziekte kan op elke leeftijd beginnen, meestal tussen de 35 en 50 jaar, maar kan tijdens de kinderjaren beginnen. Zie Juveniele idiopathische artritis .
Etiologie
Hoewel reumatoïde artritis auto-immuunreacties met zich meebrengt, is de precieze oorzaak onbekend en kunnen vele factoren bijdragen. Genetische aanleg werd geïdentificeerd in de blanke bevolking, gelokaliseerd als een epitoop in de HLA-DRB1-locus van klasse II-antigenen met histocompatibiliteit. Van onbekende of onbevestigde omgevingsfactoren (bijv. virale infecties of roken) wordt gedacht dat ze een rol spelen bij het op gang brengen en in stand houden van het gewrichtsontstekingsproces.
Pathofysiologie
Prominente immuunafwijkingen omvatten immuuncomplexen geproduceerd door synoviale membraancellen in ontstoken bloedvaten. [Plasmacellen maken antilichamen aan (bijv. reumafactor [RF], anticyclisch gecitrullineerd peptide [anti-CCP]-antilichamen) die bijdragen aan deze complexen, maar erosieve artritis kan optreden als ze afwezig zijn. Macrofagen migreren ook naar het synovium in de vroege stadia van de ziekte; toename van macrofagen, afgeleid van membraancellen, is prominent aanwezig tijdens vaatontsteking. De lymfocyten die synoviaal weefsel infiltreren zijn voornamelijk CD4+ T-lymfocyten. Macrofagen en lymfocyten produceren pro-inflammatoire cytokines en chemokines [p. bijv. Tumornecrose-tumor (TNF)-alfa, granulocyt-macrofaag-koloniestimulerende factor (GM-CSF), verschillende interleukinen, interferon-gamma] in het synovium. Het vrijkomen van ontstekingsmediatoren en verschillende enzymen draagt bij aan de systemische en gewrichtsmanifestaties van reumatoïde artritis, zoals kraakbeen- en botvernietiging ( 1 ).
Bij seropositieve reumatoïde artritis suggereert cumulatief bewijs dat anti-CCP-antilichamen verschijnen lang voordat er flogistische tekenen optreden ( 2 ). Bovendien zijn anticarbamylated antilichamen (anti-CarP) ( 3 ) meer voorspellend voor radiologische progressie bij patiënten met reumatoïde artritis en negatieve anti-CCP. Progressie naar reumatoïde artritis in de preklinische fase hangt af van de verspreiding van auto-antilichaam-epitopen waarin er immuunresponsen zijn op het vrijkomen van auto-antigenen met daaropvolgende ontsteking ( 4 ).
In chronisch aangetaste gewrichten prolifereert, verdikt en ontwikkelt het normaal gesproken delicate en dunne synoviale membraan meerdere villusplooien. De voeringcellen van het synoviale membraan produceren verschillende materialen,
zoals collagenase en stromelysine, die bijdragen aan de afbraak van kraakbeen, en interleukine-1 (IL-1) en TNF-alfa, die de afbraak van kraakbeen, osteoclast-gemedieerde botresorptie, synoviale ontsteking en prostaglandinen (die ontsteking versterken) stimuleren. Fibrine-afzettingen, fibrose en necrose zijn ook aanwezig. Door deze ontstekingsmediatoren tast hyperplastisch synoviaal weefsel (pannus) kraakbeen, subchondraal bot, gewrichtskapsel en ligamenten aan. Polymorfonucleaire lymfocyten vormen gemiddeld 60% van het aantal leukocyten in gewrichtsvloeistof.
Reumatische knobbeltjes ontwikkelen zich bij ongeveer 30% van de patiënten met reumatoïde artritis. Het zijn granulomen, met een centraal necrotisch gebied, omgeven door histiocytaire macrofagen, allemaal omhuld door lymfocyten, plasmacellen en fibroblasten. Knobbeltjes en vasculitis kunnen zich ook in veel viscerale organen ontwikkelen.
Referenties over pathofysiologie
- McInnes IB, Schett G : De pathogenese van reumatoïde artritis. N Engl J Med 365(23):2205–2219, 2011. doi:10.1056/NEJMra1004965.
- Rantapaa-Dahlqvist S, de Jong BA , Berglin E , et al : Antilichamen tegen cyclisch gecitrullineerd peptide en IgA-reumafactor voorspellen de ontwikkeling van reumatoïde artritis. Artritis Rheum 48:2741–2749, 2003. doi: 10.1002/art.11223.
- Brink M, Verheul MK, Rönnelid J, et al : Anti-carbamylated eiwit-antilichamen in de presymptomatische fase van reumatoïde artritis, hun relatie met meerdere anti-citrulline-peptide-antilichamen en associatie met radiologische schade. Artritis Res Ther 17:25, 2015. doi: 10.1186/s13075-015-0536-2.
- Sokolove J, Bromber g R, Deane KD, et al : Verspreiding van auto-antilichaamepitoop in de preklinische fase voorspelt progressie naar reumatoïde artritis. PLoS ONE 7(5):e35296, 2012. doi: 10.1371/journal.pone.0035296.
Signalen en symptomen
Het begin van reumatoïde artritis is meestal verraderlijk, beginnend met systemische en gewrichtssymptomen. Systemische symptomen zijn: ochtendstijfheid van aangetaste gewrichten, algemene vermoeidheid en malaise in de middag, anorexia, algemene zwakte en soms lichte koorts. Gewrichtssymptomen zijn pijn, zwelling en stijfheid.
Af en toe begint de ziekte plotseling en lijkt het op een acuut viraal syndroom.
De ziekte ontwikkelt zich het snelst gedurende de eerste 6 jaar, vooral het eerste jaar; 80% van de patiënten ontwikkelt binnen 10 jaar een blijvende gewrichtsafwijking. Het verloop van de ziekte is voor elke patiënt onvoorspelbaar.
Gewrichtssymptomen zijn typisch symmetrisch. Stijfheid duurt meestal > 60 minuten na het opstaan in de ochtend, maar kan optreden na langdurige inactiviteit (gelvorming genoemd). De betrokken gewrichten worden gevoelig, met erytheem, hyperthermie, oedeem en bewegingsbeperking. De belangrijkste betrokken gewrichten zijn:
Pols- en metacarpofalangeale gewrichten van de wijs- en middelvinger (meestal betrokken) Proximale interfalangeale gewrichten
Metatarsofalangeale gewrichten Schouders
Ellebogen Heupen Knieën
enkels
Vrijwel elk gewricht behalve de distale interfalangeale gewrichten (DIP’s) kan echter betrokken zijn. Het axiale skelet is zelden betrokken, met uitzondering van de cervicale wervelkolom. Synoviale verdikking is detecteerbaar. Gewrichten worden normaal gesproken in flexie gehouden om pijn te minimaliseren, wat kan leiden tot uitzetting van het kapsel.
Vaste misvormingen, met name flexiecontracturen, kunnen snel evolueren; ulnaire deviatie van de vingers met slippen van de strekpezen van de metacarpofalangeale gewrichten is typerend, evenals zwanenhals- en knoopsgatmisvormingen (zie tabel Zwanenhals- en knoopsgatmisvormingen ) . Er kan ook gewrichtsinstabiliteit zijn als gevolg van het uitrekken van het gewrichtskapsel. Carpaal tunnel syndroom kan het gevolg zijn van synovitis van de pols die op de medianuszenuw drukt. Er kunnen zich popliteale (Baker) cysten ontwikkelen, die zwelling en gevoeligheid van de kuit veroorzaken die wijzen op diepe veneuze trombose.
Extra-articulaire manifestaties
Subcutane reumatoïde knobbeltjes zijn meestal geen vroeg teken, maar ontwikkelen zich uiteindelijk bij tot 30% van de patiënten, meestal op plaatsen met chronische druk en irritatie (bijv. Extensoroppervlak van de onderarm, metacarpofalangeale gewrichten, achterhoofd). Viscerale knobbeltjes (bijv. Longknobbeltjes), meestal asymptomatisch, komen voor bij ernstige reumatoïde artritis. Longknobbeltjes van reumatoïde artritis kunnen zonder biopsie niet worden onderscheiden van longknobbeltjes van een andere etiologie.
Andere extra-articulaire symptomen zijn vasculitis , die beenulcera of mononeuritis multiplex veroorzaakt, pleurale of pericardiale effusies, longinfiltraat of fibrose, pericarditis , myocarditis , lymfadenopathie , syndroom van Felty en syndroom van Sjögren , scleromalacie en episcleritis . Betrokkenheid van de cervicale wervelkolom kan atlantoaxiale subluxatie en spinale compressie veroorzaken; subluxatie kan verergeren bij nekextensie (bijv. tijdens endotracheale intubatie). Het is vermeldenswaard dat instabiliteit van de cervicale wervelkolom meestal asymptomatisch is.
Onderhuidse reumatoïde knobbeltjes (pijl) vormen zich vaak over drukpunten, zoals bij deze patiënt met olecranon bursitis. De knobbeltjes kunnen zich in het onderhuidse weefsel bevinden dat over de bursae ligt of subperiostaal op het oppervlak van de extensor ulna.
Met toestemming van de uitgever. De Matteson E, Mason T: Atlas van reumatologie. Bewerkt door G. Hunder. Philadelphia, huidige geneeskunde, 2005.
Diagnose
Klinische criteria
Serum reumafactor (RF), anti-CCP (anticyclisch gecitrullineerd peptide) en bezinkingssnelheid van erytrocyten (bezinkingssnelheid van rode bloedcellen) of C-reactief proteïne (CRP)
Röntgenstralen
Reumatoïde artritis moet worden vermoed bij patiënten met polyarticulaire artritis en symmetrische artritis, vooral als de polsen en de 2e en 3e metacarpofalangeale gewrichten betrokken zijn. De classificatiecriteria dienen als leidraad voor het stellen van de diagnose reumatoïde artritis en zijn nuttig voor het definiëren van gestandaardiseerde behandelingspopulaties voor studiedoeleinden. De criteria hebben betrekking op resultaten van
laboratoriumtests voor reumafactor , anti-CCP en ESR of CRP (zie tabel Classificatiecriteria reumatoïde artritis ). Andere oorzaken van symmetrische polyartritis, met name hepatitis C, moeten worden uitgesloten. Patiënten moeten RF-testen, hand- en polsröntgenfoto’s en basislijnradiografie van aangetaste gewrichten ondergaan om erosieve veranderingen te documenteren. Voor patiënten met prominente lumbale symptomen moeten alternatieve diagnoses worden onderzocht.
FR’s en anti-humane globuline-antilichamen zijn aanwezig bij ongeveer 70% van de patiënten met reumatoïde artritis. RF, meestal met lage titers (niveaus kunnen variëren van laboratorium tot laboratorium), komt echter voor bij patiënten met andere ziekten, zoals andere bindweefselaandoeningen (bijv. systemische lupus erythematosus ) , granulomateuze ziekten, chronische infecties (bijv. virale hepatitis , bacteriële endocarditis , tuberculose ) en kanker. Lage RF-waarden kunnen ook voorkomen bij 3% van de algemene bevolking en 20% van de ouderen. Zeer hoge RF-titers kunnen voorkomen bij patiënten met een hepatitis C-infectie en soms bij patiënten met andere chronische infecties. Hoge latexagglutinatie RF-titers > 1:80 of een positieve anti-CCP-test ondersteunen de diagnose van reumatoïde artritis in de juiste klinische setting, maar andere oorzaken moeten worden uitgesloten.
Anticyclische gecitrullineerde peptide-antilichamen (anti-CCP, anticyclische gecitrullineerde peptide) hebben een hoge specificiteit (90%) en gevoeligheid (ongeveer 77 tot 86%) voor reumatoïde artritis en voorspellen, net als RF, een slechtere prognose. FR- en anti-CCP-waarden fluctueren niet met ziekteactiviteit. Anti-CCP-antilichamen zijn met name afwezig bij patiënten met hepatitis C die mogelijk RF-positief zijn en gewrichtszwelling hebben die verband houdt met de virale infectie.
Röntgenfoto toont alleen weke delen oedeem tijdens de eerste paar maanden van de ziekte. Dan kunnen periarticulaire osteoporose, vernauwingen en marginale erosies van de gewrichtsruimte (gewrichtskraakbeen) zichtbaar worden. Erosies ontwikkelen zich vaak binnen het eerste jaar, maar kunnen op elk moment optreden. Magnetic Resonance Imaging (MRI) lijkt gevoeliger en detecteert erosies en gewrichtsontstekingen in een vroeg stadium. Bovendien wijzen subchondrale botafwijkingen (bijv. ruggenmergletsel en zwelling) rond de knie op progressieve ziekte.
Als reumatoïde artritis wordt gediagnosticeerd, helpen aanvullende tests onverwachte complicaties en afwijkingen op te sporen. Er moet een volledig bloedbeeld met differentieel worden verkregen. Normochrome-normocytische (of licht hypochrome) anemie komt voor bij 80% van de patiënten; hemoglobine is gewoonlijk > 10 g/dl (100 g/l). Als hemoglobine ≤ 10 g/dl (100 g/l) is, moet rekening worden gehouden met een verband met ijzertekort of andere oorzaken van bloedarmoede. Neutropenie komt voor in 1 tot 2% van de gevallen, vaak met splenomegalie (syndroom van Felty). Acute fase-reactanten (bijv. Trombocytose, hoge ESR- en C-reactieve proteïnespiegels) weerspiegelen ziekteactiviteit. Milde polyklonale hypergammaglobulinemie komt vaak voor. ESR is verhoogd bij 90% van de patiënten met actieve ziekte.
Gevalideerde metingen van ziekteactiviteit zijn de DAS-28-score
van ziekteactiviteit bij reumatoïde artritis en de index van klinische ziekteactiviteit bij reumatoïde artritis.
Onderzoek van synoviale vloeistof is noodzakelijk bij elke nieuwe ontwikkeling van artritis of bij synoviale effusie om andere aandoeningen uit te sluiten en reumatoïde artritis te onderscheiden van andere inflammatoire artritis (bijv. septische artritis en kristalgeïnduceerde artritis). Bij reumatoïde artritis is de synoviale vloeistof tijdens de duur van de gewrichtsontsteking troebel, gelig en steriel en heeft gewoonlijk 10.000 tot 50.000/mL (10,0 x109 /L tot 50,0 x109 /L); typische polymorfonucleaire leukocyten overheersen, maar > 50% kunnen lymfocyten en andere mononucleaire cellen zijn. Kristallen zijn afwezig.
RF kan niet-specifiek zijn en is vaak aanwezig bij verschillende auto-immuunziekten; de aanwezigheid van anti-CCP-antilichamen (anticclisch gecitrullineerd peptide) is specifieker voor reumatoïde artritis. Hepatitis C kan bijvoorbeeld klinisch geassocieerd zijn met RF-positieve, reumatoïde-achtige artritis; anti-CCP is echter negatief.
Sommige patiënten met kristalgeïnduceerde artritis kunnen zelfs aan dezelfde criteria voldoen als reumatoïde artritis; onderzoek van de gewrichtsvloeistof verduidelijkt echter de diagnose. De aanwezigheid van kristallen maakt reumatoïde artritis onwaarschijnlijk. Gewrichtsaantasting en onderhuidse knobbeltjes kunnen het gevolg zijn van jicht, cholesterol en amyloïdose, evenals van reumatoïde artritis; punctie of biopsie van de knobbeltjes kan nodig zijn.
Systemische lupus erythematosus kan meestal worden onderscheiden als er huidlaesies zijn in gebieden die zijn blootgesteld aan licht, haar en haaruitval, orale en nasale mucosale laesies, afwezigheid van gewrichtserosie bij langdurige artritis, gewrichtsvloeistof met minder dan < 2.000 leukocyten/mcl ( 2,0 x10 9 /L) (voornamelijk mononucleaire cellen), dubbelstrengs anti-deoxyribonucleïnezuur (anti-DNA) antilichamen, nierziekte en lage niveaus van serumcomplement. In tegenstelling tot reumatoïde artritis zijn bij beeldvormingsonderzoeken de misvormingen van systemische lupus erythematosus meestal verminderd en zonder erosies en bot- of kraakbeenlaesies.
Reumatoïde artritis-achtige artritis kan ook voorkomen bij andere bindweefselaandoeningen ( bijvoorbeeld polyarteritis , sclerodermie , dermatomyositis of polymyositis ) , of er kunnen kenmerken zijn van meer dan één ziekte, wat wijst op een geassocieerd syndroom of een gemengde aandoening van het bindweefsel .
Sarcoïdose , de ziekte van Whipple , multicentrische reticulohistiocytose en andere systemische ziekten kunnen betrekking hebben op gewrichten; andere klinische kenmerken en soms weefselbiopsie helpen om deze aandoeningen te differentiëren. Acute reumatische koorts heeft een patroon van gewrichtsaandoening en bewijs van een voorgeschiedenis van streptokokkeninfectie (kweek of verandering in antistreptolysine-O-spiegels); aan de andere kant heeft reumatoïde artritis de neiging om na verloop van tijd andere gewrichten in gevaar te brengen.
Reactieve artritis kan worden onderscheiden door voorafgaande gastro-intestinale of urogenitale symptomen; asymmetrische betrokkenheid en pijn bij het inbrengen van de achillespees, het sacro-iliacale gewricht en grote gewrichten van de benen; conjunctivitis; iritis; niet-pijnlijke aften; circulerende balanitis; keratoderma blenorrhagicum op de voetzolen en elders.
Artritis psoriatica heeft de neiging asymmetrisch te zijn en wordt over het algemeen niet geassocieerd met RF, maar klinische differentiatie kan moeilijk zijn bij afwezigheid van huid- of nagellaesies. Betrokkenheid van de distale interfalangeale (DIP) gewrichten en ernstig mutilerende artritis (artritis mutilans) kunnen suggestief zijn als de aanwezigheid van oedeem in de vinger (worstvinger). Onderscheid maken tussen artritis psoriatica en reumatoïde artritis is belangrijk omdat de reactie op specifieke geneesmiddelen verschilt.
Spondylitis ankylopoetica kan worden onderscheiden door betrokkenheid van de wervelkolom en axiale gewrichten, afwezigheid van subcutane knobbeltjes en negatieve RF-test. Het HLA-B27-allel komt voor bij 90% van de blanke patiënten met spondylitis ankylopoetica.
Artrose kan worden onderscheiden door de betrokken gewrichten; de afwezigheid van reumatische knobbeltjes, systemische manifestaties of significante hoeveelheden RF en synoviaal vocht leukocytenaantal < 2.000/mcl (2,0 x109 /l). Artrose van de handen heeft meestal betrekking op de distale interfalangeale (DIP) gewrichten, de basis van de duimen en de proximale interfalangeale gewrichten en kan de metacarpofalangeale gewrichten aantasten, maar heeft meestal geen invloed op de pols. Reumatoïde artritis tast de distale interfalangeale gewrichten niet aan.
Prognose
Reumatoïde artritis verkort de levensduur met 3 tot 7 jaar, met hartaandoeningen, infectie en bloedingen gastro-intestinaal, dat verantwoordelijk is voor de meerderheid van de sterfte; medicamenteuze behandeling, kanker en andere gerelateerde ziekten kunnen verantwoordelijk zijn. Ziekteactiviteit moet worden gecontroleerd om het risico op hart- en vaatziekten bij alle patiënten met reumatoïde artritis te verminderen. (Zie ook de aanbevelingen van de European League Against Rheumatism (EULAR) voor het beheersen van het risico op hart- en vaatziekten bij patiënten met RA en andere vormen van inflammatoire gewrichtsaandoeningen.)
Ten minste 10% van de patiënten is ondanks alle behandelingen ernstig gehandicapt. Kaukasiërs en vrouwen hebben een slechtere prognose, evenals patiënten met onderhuidse knobbeltjes, gevorderde leeftijd bij aanvang van de ziekte, ontsteking in ≥ 20 gewrichten, voortijdige erosies, doorgaan met roken, hoge erytrocytsedimentatiesnelheid (RBC-sedimentatiesnelheid) en hoge niveaus van FR of anti- CCP (anticyclisch gecitrullineerd peptide).
Behandeling
Ondersteunende maatregelen (bijv. stoppen met roken, voeding, rust, lichamelijke procedures, analgetica) Geneesmiddelen die de progressie van de ziekte wijzigen
NSAID’s indien nodig voor analgesie
Behandeling van reumatoïde artritis omvat een balans tussen rust en lichaamsbeweging, goede voeding, fysieke procedures, medicijnen en soms een operatie. (Zie ook de richtlijnen van het American College of Rheumatology uit 2015 voor de behandeling van reumatoïde artritis en de EULAR – aanbevelingen uit 2019 van de European League Against Rheumatism voor de behandeling van reumatoïde artritis met synthetische en biologische aandoeningen – modificerende antirheumatische geneesmiddelen . )
levensstijl metingen
Absolute bedrust is zelden geïndiceerd, zelfs niet voor een korte periode; regelmatige rust moet echter worden aangemoedigd.
Een gemeenschappelijk voedingsdieet is geschikt. Zelden hebben patiënten exacerbaties die verband houden met specifieke voedingsmiddelen; van geen specifiek voedsel is reproduceerbaar aangetoond dat het reumatoïde artritis verergert. Dieet en voedsel voorgeschreven door niet-professionals komen vaak voor en moeten worden ontmoedigd. Het vervangen van omega-6-vetzuren (uit vlees) door omega-3-vetzuren (uit visolie) verlicht gedeeltelijk en tijdelijk de symptomen bij sommige patiënten door de productie van inflammatoire prostaglandinen te verminderen en mogelijk het darmmicrobioom te wijzigen. Stoppen met roken kan de levensverwachting verhogen.
fysieke metingen
Het gebruik van verbanden en gewrichtsspalken vermindert lokale ontstekingen en kan intense symptomen van pijn of compressieneuropathieën verlichten. Plaatselijke verkoudheid kan worden toegepast om pijn en zwelling in een gewricht te verminderen. Orthopedische schoenen en schoenen met een goede ondersteuning van de voetboog en een goede hak zijn vaak nuttig; middenvoetkussentjes die posterieur (proximaal) van de metatarsofalangeale gewrichten zijn geplaatst, verminderen de pijn door gewichtsbelasting. Bij ernstige misvormingen kunnen op maat gemaakte schoenen nodig zijn. Ergotherapie en zelfhulpmiddelen stellen patiënten met invaliderende reumatoïde artritis in staat om dagelijkse activiteiten uit te voeren.
Oefeningen moeten worden uitgevoerd wanneer dit wordt verdragen. Tijdens acute ontsteking helpt passieve bewegingsvrijheid flexiecontracturen te voorkomen. Plaatselijke warmte kan de stijfheid helpen verlichten. Bewegingsoefeningen in warm water zijn nuttig omdat de warmte de spierfunctie verbetert door stijfheid en spierspasmen te verminderen. Contracturen kunnen echter worden vermeden en de spierkracht kan het best worden hersteld nadat de ontsteking begint af te nemen; actieve oefeningen (inclusief wandelen en specifieke oefeningen voor de betrokken gewrichten) om de spiermassa te herstellen en het bewegingsbereik van de gewrichten te behouden, mogen geen vermoeidheid veroorzaken. Flexiecontracturen kunnen intensieve oefening, bracing of
immobilisatie (bijv. spalken) naar meer langgerekte posities. Paraffinebaden kunnen uw vingers opwarmen en vingeroefeningen vergemakkelijken.
Deskundige massage, tractie en diepe thermotherapiebehandeling met diathermie of echografie kunnen nuttige aanvullende therapieën zijn voor ontstekingsremmende medicijnen.
Chirurgie
Chirurgie kan worden overwogen als medicamenteuze therapie niet succesvol is. Chirurgie moet altijd worden beschouwd in termen van de totale ziekte en de verwachtingen van de patiënt. Misvormde handen en armen beperken bijvoorbeeld het gebruik van wandelstokken tijdens revalidatie; Ernstig aangetaste knieën en voeten kunnen baat hebben bij een heupoperatie. Voor elke patiënt en functie moeten redelijke doelen worden bepaald; het rechttrekken van afwijkende ulnaire vingers verbetert de handfunctie mogelijk niet. Chirurgie kan worden uitgevoerd terwijl de ziekte actief is.
Vervangende artroplastiek met gewrichtsprothese is geïndiceerd als het letsel de functie ernstig beperkt; totale heup- of knievervanging is consistent succesvol. Heup- en knieprothesen tolereren mogelijk geen krachtige activiteit (bijv. atletiekwedstrijden). Excisie van gesubluxeerde en pijnlijke metatarsofalangeale gewrichten kan het lopen enorm bevorderen. Duimfusies kunnen grijperstabiliteit bieden. Cervicale artrodese kan nodig zijn bij C1-C2-subluxatie met ernstige pijn of kans op compressie van het ruggenmerg. Artroscopie of synovectomie kan gewrichtsontsteking verlichten, maar slechts tijdelijk, tenzij de ziekteactiviteit onder controle kan worden gehouden.
Geneesmiddelen om reumatoïde artritis te behandelen
Het doel is om ontstekingen te verminderen als middel om erosies en progressieve misvormingen en verlies van gewrichtsfunctie te voorkomen. In eerste instantie worden ziektemodificerende medicijnen gebruikt, vaak in combinatie met andere medicijnen. Andere geneesmiddelenklassen lijken de progressie van RA te vertragen, waaronder biologische agentia zoals tumornecrosefactor-alfa (TNF)-antagonisten, interleukinereceptor (IL-1)-remmers, IL-6-blokkers, B-lymfocyten, modulatoren van co-stimulerende T-lymfocytmoleculen en Januskinase (JAK)-remmers. NSAID’s zijn nuttig voor het verlichten van de pijn van reumatoïde artritis, maar ze voorkomen erosie of progressie van de ziekte niet.Ze kunnen het cardiovasculaire risico verhogen en mogen daarom alleen als aanvullende therapie worden gebruikt. Laaggedoseerde systemische corticosteroïden (prednison < 10 mg eenmaal daags) kunnen worden toegevoegd om ernstige polyarticulaire symptomen onder controle te houden, meestal met als doel een RA-modificerend geneesmiddel te vervangen. Intra-articulaire depotcorticosteroïden kunnen ernstige monarticulaire symptomen of zelfs oligoarticulaire symptomen onder controle houden, maar bij regelmatig gebruik kunnen ze nadelige metabolische effecten hebben, zelfs bij lage doses.
De ideale combinatie van medicijnen is nog onduidelijk. Sommige gegevens suggereren echter dat bepaalde combinaties van geneesmiddelen uit verschillende klassen [bijv. methotrexaat met een ander disease-modifying antirheumatic drug (FARMD), snel aflopende corticosteroïden met een FARMD, methotrexaat met een TNF-alfa-antagonist of TNF-alfa-antagonist met een FARMD] zijn effectiever dan het gebruik van alleen FARMD’s opeenvolgend of met andere LANDBOUWBEDRIJVEN. Over het algemeen worden gecombineerde biologische agentia niet gegeven vanwege de verhoogde frequentie van infectie. Een voorbeeld van initiële therapie is
Geef methotrexaat 7,5 mg oraal eenmaal per week (met foliumzuur 1 mg oraal eenmaal daags).
Indien verdragen en niet adequaat, wordt de dosis methotrexaat na 3 tot 5 weken verhoogd tot een maximum van 25 mg oraal of eenmaal per week door middel van injectie (orale biologische beschikbaarheid neemt af boven 15 mg in een enkele dosis).
Als de respons niet adequaat is, moet een biologisch agens worden toegevoegd; als alternatief is drievoudige therapie met methotrexaat, hydroxychloroquine en sulfasalazine een optie.
Leflunomide kan worden gebruikt in plaats van methotrexaat of toegevoegd aan methotrexaat met nauwlettende controle van serumtransaminasespiegels en CBC.
Niet-steroïde anti-inflammatoire geneesmiddelen (NSAID’s)
Acetylsalicylzuur wordt niet langer gebruikt voor reumatoïde artritis omdat effectieve doses vaak giftig zijn. Er mag slechts één NSAID per periode worden gegeven ( zie Behandeling van reumatoïde artritis met niet-steroïde anti-inflammatoire geneesmiddelen (NSAID’s ) ), hoewel patiënten ook acetylsalicylzuur ≤ 325 mg/dag kunnen gebruiken voor een cardioprotectief plaatjesaggregatieremmend effect. Aangezien de maximale respons op NSAID’s tot 2 weken kan duren, moeten de doses met dezelfde frequentie worden verhoogd. Medicijndoses met flexibele doseringen kunnen worden verhoogd totdat de respons wordt bereikt met minimale of maximale dosering. Alle NSAID’s behandelen de symptomen van reumatoïde artritis en verminderen ontstekingen, maar ze veranderen het verloop van de ziekte niet en daarom mogen ze alleen adjuvans worden gebruikt.
NSAID’s remmen cyclo-oxygenase (COX)-enzymen en verminderen de prostaglandineproductie. Sommige prostaglandinen onder controle van COX-1 hebben belangrijke effecten in veel delen van het lichaam (bescherming van het maagslijmvlies en remming van de hechting van bloedplaatjes). Andere prostaglandinen worden geïnduceerd door ontsteking en worden geproduceerd door COX-2. Selectieve COX-2-remmers, ook wel coxibs genoemd (bijv. celecoxib), lijken een vergelijkbare werkzaamheid te hebben als niet-selectieve NSAID’s en veroorzaken iets minder gastro-intestinale toxiciteit; maar niet minder waarschijnlijk nefrotoxiciteit veroorzaken. Celecoxib 200 mg oraal eenmaal daags heeft een cardiovasculair veiligheidsprofiel dat vergelijkbaar is met dat van niet-selectieve NSAID’s. Het blijft onduidelijk of een volledige dosis celecoxib (200 mg oraal tweemaal daags) cardiovasculaire risico’s heeft die vergelijkbaar zijn met die van niet-selectieve NSAID’s.
NSAID’s, behalve misschien coxibs, moeten worden vermeden bij patiënten met een maagzweer of dyspepsie; maagzuur onderdrukkende therapie moet worden gegeven aan deze patiënten. Andere mogelijke bijwerkingen van alle NSAID’s zijn hoofdpijn, verwardheid en andere symptomen van het centrale zenuwstelsel verhoogde bloeddruk, verergering van hypertensie, oedeem en verminderde bloedplaatjesfunctie; celecoxib heeft echter geen significant plaatjesaggregatieremmend effect. NSAID’s verhogen het cardiovasculaire risico ( zie Niet-opioïde analgetica ) . Creatininespiegels kunnen onomkeerbaar stijgen als gevolg van remming van nierprostaglandinen en verminderde nierbloedstroom; minder vaak kan interstitiële nefritis optreden. Patiënten met urticaria, rhinitis of astma veroorzaakt door acetylsalicylzuur kunnen hetzelfde probleem hebben met deze andere NSAID’s, maar celecoxib veroorzaakt deze problemen mogelijk niet.
NSAID’s moeten in de laagst mogelijke dosis worden gebruikt om hun nadelige effecten te verminderen.
Disease-modifying anti-reumatic drugs (FARMD’s)
( Andere geneesmiddelen die worden gebruikt om reumatoïde artritis te behandelen voor informatie over de specifieke dosering en bijwerkingen van andere geneesmiddelen die worden gebruikt om reumatoïde artritis te behandelen.)
FARMD lijkt de voortgang van reumatoïde artritis te vertragen en is geïndiceerd bij bijna alle patiënten met reumatoïde artritis. Ze verschillen chemisch en farmacologisch van elkaar. Bij veel duurt het weken of maanden voordat ze effect hebben. Ongeveer tweederde van de patiënten ervaart een verbetering van de algemene toestand, maar volledige remissies komen vaker voor. Veel FARMD’s resulteren in bewijs van schadebeperking in beeldvormingsstudies, vermoedelijk als gevolg van verminderde ziekteactiviteit. Patiënten moeten volledig worden voorgelicht over de risico’s van ziektemodificerende geneesmiddelen en nauwlettend worden gecontroleerd op tekenen van toxiciteit.
Bij het kiezen van FARMD’s moeten de volgende principes in overweging worden genomen:
Combinaties van FARMD’s kunnen effectiever zijn dan afzonderlijke medicijnen. Zo zijn hydroxychloroquine, sulfasalazine en methotrexaat samen effectiever dan alleen methotrexaat of twee andere combinaties.
Het combineren van een FARMD met een ander geneesmiddel, zoals methotrexaat samen met een tumornecrosefactor (TNF)-alfa-antagonist of een snel stopgezette corticosteroïde, kan effectiever zijn dan het gebruik van alleen FARMD’s.
Methotrexaat is een folaatantagonist met immunosuppressieve effecten bij hoge doses. Het heeft een ontstekingsremmende werking bij de doses die worden gebruikt bij reumatoïde artritis. Het is zeer effectief en begint relatief snel (klinisch voordeel meestal binnen 3 tot 4 weken). Methotrexaat moet, indien nodig, met voorzichtigheid worden gebruikt bij patiënten met leverdisfunctie of nierinsufficiëntie. Alcohol moet worden vermeden. Aanvullend foliumzuur, eenmaal daags oraal 1 mg, kan de kans op bijwerkingen verminderen. Een volledig bloedbeeld en serumspiegels van aspartaataminotransferase (AST), alanineaminotransferase (ALT), albumine en creatinine moeten ongeveer elke 8 weken worden gemeten. Bij gebruik in een vroeg stadium van reumatoïde artritis kan de effectiviteit gelijk zijn aan die van biologische middelen. Leverbiopsie kan nodig zijn als levertesten aanhoudend tweemaal het normale bereik zijn en de patiënt methotrexaat moet blijven gebruiken.
Ernstige terugval van artritis kan optreden na stopzetting van het gebruik van methotrexaat. Paradoxaal genoeg kunnen reumatoïde knobbeltjes toenemen bij gebruik van methotrexaat.
Hydroxychloroquine kan ook de symptomen van milde reumatoïde artritis onder controle houden. Fundus- en gezichtsveldonderzoeken moeten tijdens de behandeling om de 12 maanden worden uitgevoerd. Het medicijn moet worden stopgezet als er na 9 maanden geen verbetering is.
Sulfasalazine kan de symptomen verbeteren en de progressie van gewrichtsschade vertragen. Over het algemeen zijn het gecoate tabletgegevens. De voordelen zouden binnen 3 maanden moeten optreden. Een omhulde tablet of dosisverlaging kan de verdraagbaarheid verhogen. Omdat neutropenie vroeg kan optreden, moeten bloedtellingen na 1 tot 2 weken en vervolgens elke 12 weken tijdens de behandeling worden verkregen. AST en ALT moeten worden verkregen met tussenpozen van 6 maanden en telkens wanneer de dosis wordt verhoogd.
Leflunomide interfereert met een enzym dat betrokken is bij het metabolisme van pyrimidine. Het is bijna net zo effectief als methotrexaat, maar veroorzaakt minder snel beenmergdepressie, abnormale leverfunctie en longontsteking. Alopecia en diarree komen vrij vaak voor bij het begin van de therapie, maar kunnen verdwijnen bij voortzetting van de therapie.
Parenterale goudzouten worden niet meer gebruikt.
corticoïden
Systemische corticosteroïden verminderen ontstekingen en andere symptomen sneller en beter dan andere geneesmiddelen. Ze lijken ook boterosie te verminderen. Het is echter mogelijk dat ze de vernietiging van gewrichten niet voorkomen, en hun klinische voordeel neemt over het algemeen met de tijd af. Bovendien volgen ernstige rebound-effecten bij stopzetting van corticosteroïden bij actieve ziekte. Vanwege hun nadelige effecten op de lange termijn, bevelen sommige clinici aan dat corticosteroïden alleen worden gegeven om de functie te behouden totdat andere FMARD’s effect hebben.
Corticosteroïden kunnen worden gebruikt om verschillende ernstige articulaire of systemische manifestaties van reumatoïde artritis te behandelen (bijv. vasculitis, pleuritis, pericarditis). Contra-indicaties zijn maagzweren, hypertensie, onbehandelde infecties, diabetes mellitus en glaucoom. Het risico op tuberculose moet vooraf worden overwogen therapie met corticosteroïden begint.
Intra-articulaire injecties met corticosteroïden kunnen tijdelijk helpen pijn en zwelling in bijzonder pijnlijke gewrichten onder controle te houden. Triamcinolonhexacetonide kan ontstekingen gedurende langere tijd onderdrukken. Triamcinolonacetonide en methylprednisolonacetaat zijn ook effectief. Elk geïsoleerd gewricht mag niet meer dan 3 tot 4 keer per jaar worden geïnfiltreerd met corticosteroïden, aangezien frequente infiltraties de gewrichtsvernietiging kunnen versnellen (hoewel er geen patiëntspecifieke gegevens zijn om dit te bewijzen). Omdat injecteerbare corticosteroïde-esters kristallijn zijn, neemt lokale ontsteking tijdelijk toe binnen een paar uur bij <2% van de injecties bij patiënten die injecties krijgen. Hoewel infectie slechts voorkomt bij < 1:40.000 van de patiënten, moet er rekening mee worden gehouden als er pijn is > 24 uur na infiltratie.
Cytotoxische, immunosuppressieve of immunomodulerende geneesmiddelen
Behandeling met azathioprine, cyclosporine (een immunomodulerend geneesmiddel) heeft een vergelijkbare werkzaamheid als FARMD. Deze medicijnen zijn echter giftiger. Dergelijke medicijnen worden dus alleen gebruikt voor patiënten bij wie de behandeling met FARMD is mislukt of om de behoefte aan corticosteroïden te verminderen. Ze worden niet vaak gebruikt, tenzij er extra-articulaire complicaties zijn. Bij onderhoudstherapie met azathioprine dient de laagste effectieve dosis te worden gebruikt. Een lage dosis ciclosporine kan alleen of in combinatie met methotrexaat effectief zijn, maar wordt zelden gebruikt. Mogelijk minder toxisch dan azathioprine. Cyclofosfamide wordt niet langer aanbevolen vanwege de toxiciteit.
Biologische middelen
Biologische responsmodificatoren kunnen worden gebruikt in plaats van tumornecrosefactor (TNF)-alfa-antagonisten om zich op B-cellen of T-cellen te richten. Deze middelen worden doorgaans niet met elkaar gecombineerd.
Rituximab is een anti-CD20-antilichaam dat B-cellen uitput. Het kan worden gebruikt bij refractaire patiënten. Vaak is de reactie traag, maar het kan 6 maanden duren. De cursus kan na 6 maanden worden herhaald. Milde bijwerkingen komen vaak voor en analgesie, corticosteroïden, difenhydramine of een combinatie hiervan kunnen gelijktijdig worden gegeven. Het gebruik van rituximab is meestal beperkt tot patiënten bij wie geen verbetering is opgetreden na gebruik van een TNF-alfaremmer en methotrexaat. Behandeling met rituximab is in verband gebracht met progressieve multifocale leuko-encefalopathie, mucocutane reacties, laat optredende leukopenie en hepatitis B-reactivatie.
Abatacept , een oplosbare cytotoxische fusie van T-lymfocyt-geassocieerd antigeen 4 (CTLA-4), is geïndiceerd voor patiënten met reumatoïde artritis die onvoldoende reageren op andere FARMD’s.
Anakinra is een recombinante interleukine-1 (IL-1)-receptor. IL-1 is sterk betrokken bij de pathogenese van reumatoïde artritis. Infectie en leukopenie kunnen problemen zijn. Het wordt minder vaak gebruikt omdat het elke dag moet worden gegeven.
Tumornecrosefactor (TNF)-alfa-antagonisten (bijv. adalimumab, golimumab, certolizumab pegal, infliximab en hun biosimilars) kunnen de erosieprogressie en het aantal nieuwe erosies verminderen. Hoewel niet alle patiënten reageren, voelen velen een gevoel van welzijn, soms al bij de eerste infiltratie. Ontsteking wordt vaak radicaal verminderd. Deze medicijnen worden vaak toegevoegd aan methotrexaattherapie om het effect te versterken en mogelijk de aanmaak van medicijnneutraliserende antilichamen te voorkomen.
Recente informatie suggereert veiligheid tijdens de zwangerschap met de FTN-remmers en anakinra. TNF-alfa-antagonisten moeten waarschijnlijk vóór een grote operatie worden stopgezet om het risico op preoperatieve infectie te verkleinen. Etanercept, infliximab en adalimumab kunnen met of zonder methotrexaat worden gebruikt. TNF-remmers kunnen vatbaar maken voor hartfalen en zijn daarom relatief gecontra-indiceerd bij stadium 3 en 4 hartfalen. Het risico op lymfoom is niet verhoogd bij RA-patiënten die worden behandeld met TNF-remmers ( 1 ).
Sarilumab is een interleukine-6 (IL-6)-remmer. Het is beschikbaar voor volwassenen met matige tot
ernstig actief die onvoldoende hebben gereageerd op een of meer FARMD’s of deze niet kunnen verdragen.
Tocilizumab is een IL 6-remmer en heeft klinische werkzaamheid bij patiënten die een onvolledige respons hebben gehad op andere biologische agentia.
Baricitinib is een orale Januskinase (JAK)-remmer. Het is geïndiceerd voor volwassenen met matig tot ernstig actieve reumatoïde artritis die onvoldoende reageren op een of meer TNF-antagonisten.
Tofacitinib is een JAK-kinase (QJ)-remmer die oraal wordt toegediend met of zonder gelijktijdig methotrexaat voor patiënten die niet reageren op methotrexaat alleen of op andere biologische geneesmiddelen.
Upadacitinib is een oraal toegediende JAK-remmer voor volwassenen met matig tot ernstig actieve reumatoïde artritis die onvoldoende hebben gereageerd op of intolerant zijn voor methotrexaat. Andere JAK-remmers die mogelijk binnenkort beschikbaar komen in de VS zijn filgotinib en peficitinib.
Hoewel er enkele verschillen zijn tussen middelen, is infectie het ernstigste probleem, vooral bij reactieve tuberculose. Patiënten moeten worden gescreend op tuberculose met behulp van gezuiverde eiwitderivaten (DPP)-testen of een interferon-gamma-afgiftetest. Andere ernstige infecties kunnen optreden, zoals sepsis, diepe mycosen en infecties veroorzaakt door andere opportunistische organismen.
Bibliografische referentie
Minozzi S, Bonovas S, Lytras T, et al : Risico op infecties met behulp van anti-TNF-middelen bij reumatoïde artritis, psoriatische artritis en spondylitis ankylopoetica: een systematische review en meta-analyse. Expert Opin Drug Saf 15(sup1):11–34, 2016. doi: 10.1080/14740338.2016.1240783.